2019年以来m6A RNA甲基化在各个领域都有新的重大突破, 8月份(Epub时间最早也在8月份)以来10分以上文章共计8篇,7-10分档2篇,现将该10篇文章做如下总结,包含病毒、免疫、动植物、自噬、肿瘤、骨生长等研究方向,更重要的是科研热点与热点的结合,如单细胞与m6A,相分离与m6A,CRISPR与m6A,自噬与m6A。
CNS级别—病毒、免疫与m6A

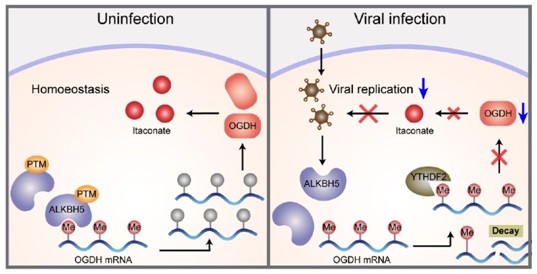
8月份CNS级别仅有1篇Science文章,来自于南开大学曹雪涛院士课题组,研究发现N6-甲基腺嘌呤(m6A)修饰参与调控宿主细胞代谢重塑从而抑制病毒复制。机制上,宿主细胞为应对病毒感染会抑制m6A去甲基化酶ALKBH5的活性,由此增加了α-酮戊二酸脱氢酶(OGDH) mRNA的m6A修饰,进而降低了OGDH mRNA稳定性和蛋白水平。OGDH降低后又减少了代谢物衣康酸的产生,而衣康酸对于病毒复制是必需的。研究进一步发现ALKBH5缺陷的小鼠可以不依赖天然免疫的方式来抵御病毒感染,因此从RNA表观修饰的角度为了解非天然免疫方式应对病毒入侵提供了新的思路,也为控制病毒感染寻找新的潜在靶点提供了重要依据!
而在今年7月份,曹雪涛院士团队在Science上以长文形式发表了题为Nuclear hnRNPA2B1 initiates and amplifies the innate immune response to DNA viruses的研究论文,与上边不同的是,这篇文章发现了DNA感受器蛋白hnRNPA2B1以先天免疫方式应对DNA病毒感染。hnRNPA2B1能够识别病毒DNA,二聚体化后被精氨酸去甲基化酶JMJD6去甲基化,然后被转运至细胞质中并最终导致INF -α/β的产生。另外hnRNPA2B1能够促进CGAS, IFI16和STING mRNAs的m6A修饰及核质转运等,在病毒感染后能够通过影响m6A修饰方式进一步确保INF -α/β的产生。(hnRNPA2B1已被报道可作为pri-miRNA m6A修饰的reader蛋白,Cell, 2015)

Cell Reports—单细胞与m6A

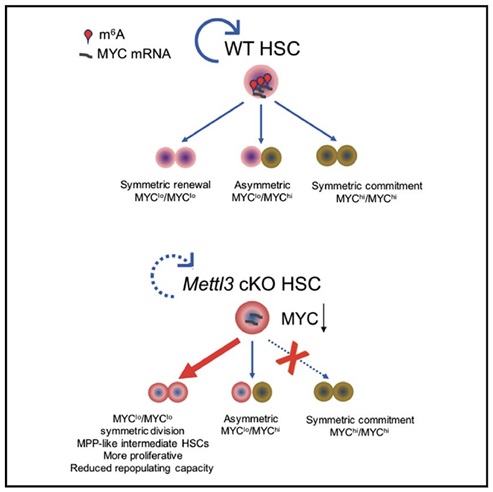
纪念斯隆-凯特琳癌症中心的科研人员发现m6A RNA甲基化能够维持造血干细胞的身份和对称分化(m6A RNA Methylation Maintains Hematopoietic Stem Cell Identity and Symmetric Commitment)。干细胞的对称分化对于组织损伤或压力条件下的快速再生是至关重要的。研究人员利用m6A甲基转移酶Mettl3条件性敲除的老鼠和对照老鼠进行研究,结合单细胞RNA测序和转录组测序发现m6A缺陷的造血干细胞(HSCs)不能进行对称性分化。机制上,在分化的HSCs中RNA甲基化调控着Myc mRNA的丰度,而且MYC可以作为HSC不对称和对称分化的marker。
Cell Research—相分离与m6A

2019年8月清华大学生科院李丕龙研究员团队在Cell Research上以Letter的形式发表了题为Multivalent m6A motifs promote phase separation of YTHDF proteins的论文,揭示了含有多价m6A motifs的RNA能够增强YTHDF蛋白的相分离潜能。数据表明m6A和YTHDF2的相分离与细胞对压力的反应相关,m6A修饰的功能多种多样,其中很多都是通过m6A的识别蛋白来实现的,而多价的m6A驱动的YTHDFs相分离可能对其功能的实现有重要作用。
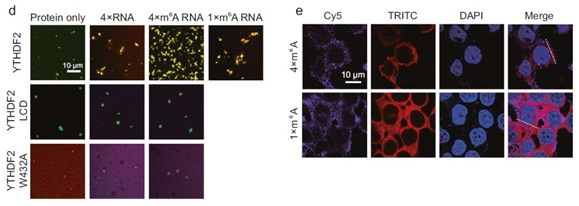
而在今年7月份康奈尔大学研究团队率先在Nature上报道称m6A修饰能够增强mRNA的相分离,特别是在含有多个m6A残基的条件下。
NCB—CRISPR与m6A

8月5日美国康奈尔大学钱书兵教授团队在Nature Chemical Biology上发表的论文报道了“新开发的m6A编辑工具能够在不改变基本序列的前提下实现对m6A修饰的写入和擦除”,主要通过融合CRISPR-Cas9和m6A甲基转移酶/去甲基转移酶实现对不同的mRNA区域单个位点的甲基化写入或擦除。这项工作对表观转录组机制的理解具有重大意义。
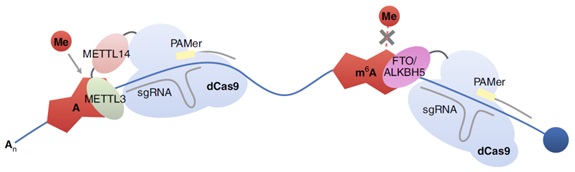
同时何川教授对该项工作予以高度评价:“这项新的方法基于CRISPR技术调控mRNA中的m6A修饰水平,能够更加直接地从功能上理解位点特异性的m6A修饰”,“同时可能对了解cap-m6Am在特定转录本或特定生物学过程中的功能具有重大作用”。

Autophagy——自噬与m6A

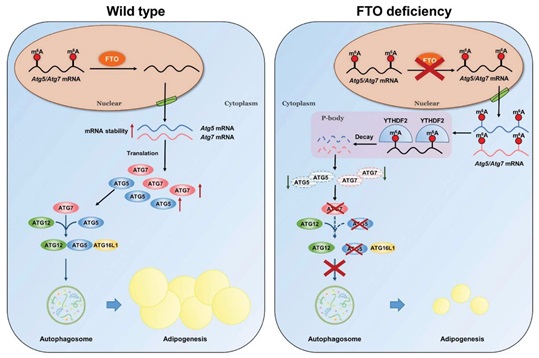
浙江大学动物科学学院汪以真教授团队于8月26日在Autophagy杂志上发表了m6A mRNA methylation controls autophagy and adipogenesis by targeting Atg5 and Atg7的论文,发现m6A mRNA甲基化能够通过靶向Atg5和Atg7调控自噬和脂肪生成。机制上围绕FTO这一去甲基转移酶进行敲降,发现ATG5和ATG7转录本的表达水平下降依赖于m6A修饰的方式,导致自噬小体的形成减弱,因而抑制了自噬和脂肪形成;进一步发现Atg5和Atg7作为YTHDF2这一reader的靶点,FTO沉默后,捕获YTHDF2后发现Atg5和Atg7转录本具有更高的m6A水平,导致mRNA降解及蛋白水平的下降。在FTO敲除小鼠中同样验证了这一机制,因此这些结果能够说明m6A RNA甲基化修饰对于自噬和脂肪形成的重要作用。
动植物与m6A

2019年8月5日Nature Microbiology上在线发表了法国巴斯德研究所的题为Transcriptome-wide dynamics of extensive m6A mRNA methylation during Plasmodium falciparum blood-stage development的论文,发现了恶性疟原虫在红内期(blood-stage)进展过程中存在广泛的m6A mRNA甲基化修饰。研究人员利用质谱和m6A RNA测序证实了m6A的广泛存在,而且随发展进程被调控,并且远超过其它真核生物中的m6A水平。同时发现了一个潜在的m6A甲基化转移酶PfMT-A70,利用CRISPR干扰后显著增加转录本水平;而且进一步识别了两种可能的m6A结合的YTH蛋白。这些结果证实了疟原虫中广泛的m6A修饰的特征,并且显示了单细胞真核生物m6A修饰在转录动态微调中的关键作用。

2019年8月6日中科院植物研究所秦国政研究组和田世平研究组合作,于Genome Biology期刊上揭示了DNA甲基化可通过调节m6A去甲基化酶基因表达的方式影响番茄果实m6A修饰,而m6A去甲基化酶反馈调节DNA甲基化,从而共同调控果实成熟。m6A修饰普遍存在于番茄果实mRNA中,主要发生在终止密码子附近和3’非翻译区。总体而言,m6A修饰与转录本水平呈负相关。研究进一步证实了在Cnr突变体(成熟缺陷)中m6A整体水平的增加与m6A去甲基化酶基因SlALKBH2的表达下降有关;而SlALKBH2受DNA甲基化调控。有意思的是,m6A去甲基化酶SlALKBH2能够结合DNA去甲基化酶基因SlDML2的mRNA,并且调节其m6A修饰及稳定性。SlALKBH2基因突变后SlDML2的m6A水平升高,mRNA含量降低,果实不能正常成熟。

肝癌与WTAP

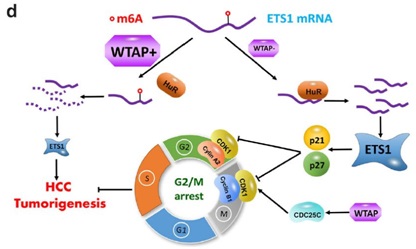
在肝癌领域已经有几篇文章报道m6A修饰参与肝癌的进展过程中,包括METTL3 (Hepatology, 2018)、METTL14 (Hepatology, 2017)、IGF2BP (Nucleic Acids Research, 2019)等。浙大附属第一医院肝胆胰外科郑树森院士团队围绕m6A甲基转移酶复合物之一WTAP,研究其参与肝细胞癌进展的机制,相关成果发表在2019年8月22日的Molecular Cancer上。结果发现WTAP在HCC中呈高表达,与不良预后相关,而且其表达水平能够单独预测HCC生存期。功能上WTAP能够在in vitro/in vivo条件下促进HCC细胞增殖和肿瘤生长。机制上,ETS1被发现作为WTAP的下游因子,WTAP能够通过m6A修饰在转录后抑制ETS1,同时有HuR的参与。而ETS1能够抑制HCC进展,并且能够rescue WTAP缺陷影响的表型。而且WTAP通过受ETS1调控的p21/p27依赖的方式影响HCC细胞周期。总体上,这篇文章首次报道WTAP调控m6A甲基化修饰在肝癌肿瘤发生中的作用,WTAP可能作为HCC潜在的治疗靶点。
NC—热休克反应与m6A

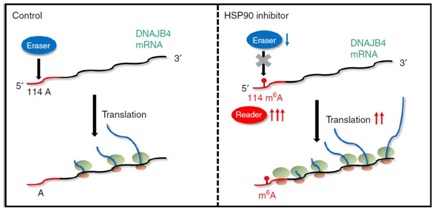
美国加州大学河滨分校汪寅生教授团队发现热休克蛋白HSP90抑制剂能够通过m6A修饰的机制刺激DNAJB4蛋白的表达,而且m6A的表观修饰机制能够被writer, eraser和reader蛋白调控。相关研究结果发表在2019年8月9日的Nature Communications上。
PNAS—骨量与FTO

约翰霍普金斯大学研究团队为了研究FTO(脂肪量和肥胖相关基因)在骨中的作用,分别利用FtoKO和Fto
Oc KO(骨细胞选择性敲除)的小鼠研究表型的影响。两种小鼠模型均会导致骨小梁和皮质中随年龄相关的骨量的减少。成骨细胞中Hspa1a和其它DNA修复通路中的基因的转录本水平会受Fto的影响,而且这些基因中含有的m6A motifs受Fto的去甲基化修饰的调控。而在Fto KO的成骨细胞中过表达Hspa1a或抑制NF-κB信号通路能够恢复DNA损伤和凋亡速率。进一步用高脂饮食诱导增加小鼠代谢压力,Fto Oc KO小鼠显示出比正常小鼠更大的DNA损伤。这些数据表明在成骨细胞中FTO功能上能够通过Hspa1a-NF-κB信号通路增强一些mRNA的稳定性,而这些基因的蛋白能够保护细胞免受遗传毒性的损伤。
关于天昊
天昊生物具有多年基因组、转录组和表观组等多组学检测与分析的经验,m6A RNA甲基化作为表观领域的一大热点,天昊生物可为您提供m6A整体水平定量,结合RNA-seq和m6A MeRIP-seq挖掘潜在的受m6A调控酶影响的靶点,同时可对靶点进行MeRIP-qPCR验证。生信团队亦可提供个性化的数据库挖掘与生信分析内容。欢迎联系我们!邮箱:techsupport@geneskies.com电话:400-065-6886