上一期我们对5篇肝癌单细胞转录组文章的内容进行了简单总结,本期集中在乳腺癌上。根据最新的乳腺癌综述文章报道:乳腺癌是全球女性最常见的恶性肿瘤,约70-80%的早期非转移性疾病患者可治愈。晚期乳腺癌伴远端器官转移被认为是目前可用的治疗方法所无法治愈的。在分子水平上,乳腺癌是一种异质性疾病,其分子特征包括人表皮生长因子受体2 (HER2, ERBB2编码)的激活,激素受体(雌激素受体和孕激素受体)的激活和/或BRCA突变。治疗策略根据分子亚型的不同而不同(Nat Rev Dis Primers, 2019 Sep 23)。
以(((((transcriptome) OR transcriptomics) OR RNA sequencing) OR RNA-seq) AND single cell) AND breast cancer作为关键词,通过PubMed检索发现多篇文章涉及到乳腺癌的单细胞转录组研究,精选了其中6篇CNS系列文章,5篇Nature Communications,1篇Genome Biology和1篇Cell Reports。
(一)

这篇文章发表在2014年8月的Cell上,利用早期的单细胞转录组方法比较了乳腺癌患者的15个单个CTC细胞和14个CTC clusters的转录组信息。
主要内容:循环肿瘤细胞簇(CTC簇)存在于癌症患者的血液中,但其对转移的贡献尚不明确。利用标记了乳腺肿瘤的小鼠模型,我们证明了CTC簇来自于寡克隆的肿瘤细胞群,而不是来自于血管内聚集事件。虽然与单个CTC相比,CTC簇在血液中比较少见,但CTC簇增加了23-50倍的转移潜能。在10位转移性乳腺癌患者中,对来源于同一样本配对的CTC簇和单个CTCs进行单细胞分辨率RNA测序(方法参考2010年汤富酬Nature Protocols),发现细胞连接成分高表达的盘状球蛋白(plakoglobin)。在小鼠模型中,敲低plakoglobin可抑制CTC簇的形成并抑制肺转移。在乳腺癌患者中,CTC簇的丰度和高的肿瘤盘状球蛋白水平都提示了不良结果。因此,CTC簇是由原发肿瘤细胞的多细胞群通过plakoglobin依赖的细胞间黏附结合在一起而形成的,虽然罕见,但它们对癌症的转移扩散起了重要作用。
(二)
2019年2月这篇Nature在研究对象上与前边提到的2014年8月份的Cell较为接近,同样揭示了CTC相关的cluster在促进乳腺癌转移过程中的重要作用。
主要内容:更好地理解定义癌细胞和免疫细胞之间相互作用的特征对于开发新的癌症治疗方法是很重要的。然而,重点往往放在了原发肿瘤及其微环境的相互作用上,而免疫细胞在患者的癌症散播过程中的作用很大程度上仍未确定。循环肿瘤细胞(CTCs)是一些癌种转移的前体细胞(precursors),有时可在血液中与非恶性细胞,如白细胞(WBCs)结合。这些CTC结合的WBCs的身份和功能,以及定义WBCs和CTCs相互作用的分子特征均是未知的。在此,我们从乳腺癌患者和小鼠模型中分离并鉴定了单个CTC相关的WBCs,以及与每个CTC-WBC簇相对应的癌细胞。我们使用单细胞RNA测序显示出在大多数病例中CTCs与中性粒细胞相关(Smart-seq2)。在比较中性粒细胞相关的CTCs与单独的CTCs的转录组特征时,我们发现了一些差异表达的基因,它们勾勒出细胞周期进展,导致更有效的转移形成。此外,我们确定了细胞与细胞连接和细胞因子与受体对,其定义了CTC和中性粒细胞群,代表了转移过程的关键缺陷。因此,中性粒细胞和CTC之间的联系在血液中驱动了细胞周期进展,并扩展了CTC的转移潜能,为靶向这种相互作用治疗乳腺癌提供了理论基础。
(三)

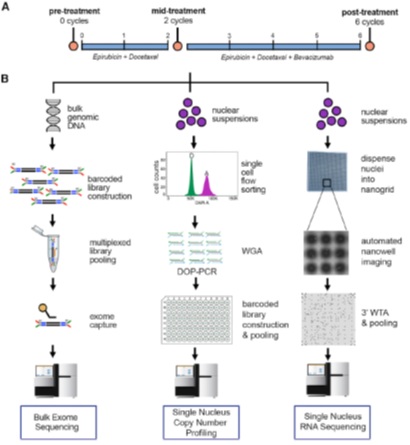
2018年5月份的这篇Cell主要结合单细胞核的DNA测序、单细胞RNA测序和bulk外显子测序分析治疗进展的样本中化疗影响的基因组和转录组信息的变化。
主要内容:三阴性乳腺癌(TNBC)是乳腺癌中一种侵袭性的亚型,常对化疗产生耐药性。一个尚未解决的问题是,抗性是由罕见的已存在的克隆选择引起的,还是通过获取新的基因组畸变引起的。为了研究这个问题,我们对20例TNBC患者进行新辅助化疗(NAC)期间的纵向样本进行单细胞核DNA和RNA测序(参考2017年NC文章)、bulk外显子测序。深度的外显子测序发现10例患者NAC导致克隆的消失,而10例患者在治疗后克隆依旧存在。在8例患者中,我们进行了更详细的研究,使用单细胞DNA测序分析了900个细胞,单细胞RNA测序分析了6862个细胞。我们的数据显示耐药基因型是预先存在的,并且通过NAC进行适应性选择,而转录组特征则是通过对TNBC患者化疗的反应进行重编程而获得的。
(四)

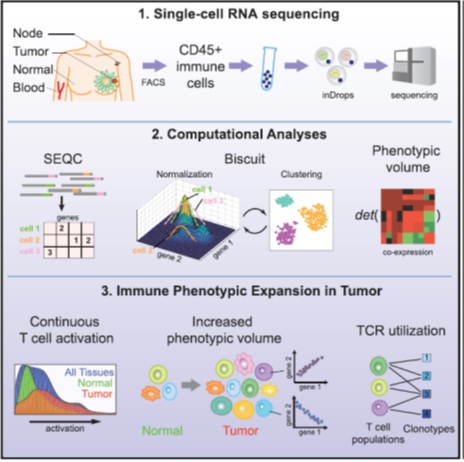
2018年8月的Cell分别用两种单细胞RNA测序平台解析了乳腺癌免疫细胞表型多样性的原因,展示了乳腺癌免疫微环境图谱。
主要内容:了解肿瘤微环境中的免疫细胞表型对于理解肿瘤进展机制和免疫治疗反应是至关重要的。我们使用单细胞RNA-seq分析了8例乳腺癌中的45000个免疫细胞(CD45+),包括正常乳腺组织、血液和淋巴结样本(inDrop平台)。我们开发了预处理流程—SEQC,以及贝叶斯聚类和标准化方法—Biscuit,以解决单细胞数据固有的计算挑战。尽管在正常和肿瘤组织免疫细胞之间有显著的相似性,但我们观察到肿瘤微环境特异的持续表型扩张。分析27,000个额外CD3+ T细胞配对的单细胞RNA测序和T细胞受体(TCR)测序数据(10x平台),揭示了TCR利用对表型多样性的组合的影响。我们的研究结果支持了T细胞持续激活的模型,但与癌症巨噬细胞极化模型不一致。我们的研究结果对肿瘤浸润免疫细胞的表征具有重要意义。
(五)

2018年6月的Nature Medicine利用10x单细胞平台展示了乳腺癌中肿瘤浸润性T细胞的异质性,转录组信息可以用于分子特征发现和预后评价。
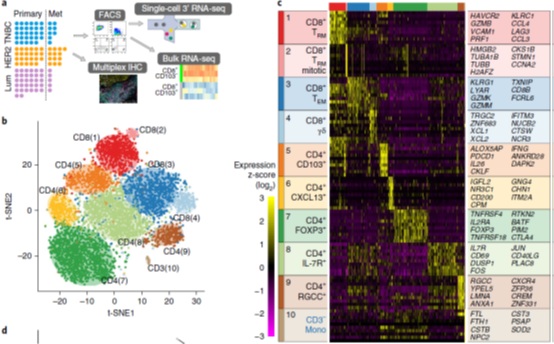
主要内容:乳腺癌(BC)中肿瘤浸润淋巴细胞(TILs)的数量是改善患者生存的一个强有力的预后指标,特别是在三阴性和HER2过表达的BC亚型中。虽然T细胞在TIL群中占主导地位,但T细胞亚群的数量和质量差异与患者预后之间的关系仍不清楚。我们对人BCs中分离的6,311个T细胞进行了单细胞RNA测序(scRNA-seq),结果显示浸润的T细胞群存在显著的异质性(10x平台)。我们证明了具有高数量TILs的BCs含有的CD8+ T细胞具有组织常驻记忆T (TRM)细胞分化特征的,这些CD8+ TRM细胞表达了高水平的免疫检查点分子和效应蛋白。根据scRNA-seq数据获得的一个CD8+ TRM基因特征与早期三阴性乳腺癌(TNBC)患者生存期的改善显著相关,且其预后优于单独的CD8表达。我们的数据表明CD8+ TRM细胞参与了BC的免疫监测,是免疫检查点抑制调控的关键靶点。进一步了解TRM细胞的发育、维持和调控对乳腺癌成功的免疫治疗的开发至关重要。
(六)

2018年12月的Cancer Cell文章借助于单细胞分析确定了内分泌抗性是由于选择一个预先存在的独特的细胞群,转录组的异质性与耐药有关,表观治疗的药物可能对癌症治疗有关键作用。
主要内容:KDM5组蛋白H3赖氨酸4去甲基化酶家族成员与治疗耐药相关,包括乳腺癌的内分泌抗性,但其潜在机制尚不明确。我们发现KDM5A/B的遗传缺失或KDM5活性的抑制通过调控雌激素受体(ER)信号和减少细胞转录组异质性来增加抗雌激素的敏感性。KDM5B的高表达与ER+乳腺肿瘤的高转录组异质性和不良预后有关。单细胞RNA测序(inDrop平台)、细胞条形码(barcoding)和数学模型证实了内分泌抗性是由于选择已有的遗传上不同的细胞,而KDM5抑制剂抗性是后天获得的。我们的发现强调了细胞表型异质性在耐药中的重要性,并确定KDM5A/B是这一过程的关键调控因子。
天昊生物
天昊生物具有多年基因组、转录组和表观组等多组学检测与分析的经验,现推出的10x Genomics单细胞转录组测序可为您提供专业的科研服务及个性化的单细胞信息挖掘,期待成为您单细胞测序分析的优质服务提供商!
欢迎联系我们具体咨询!
邮箱:techsupport@geneskies.com