英文题目: Mediterranean diet intervention alters the gut microbiome in older people reducing frailty and improving health status: the NU-AGE 1-year dietary intervention across five European countries
中文题目:地中海饮食干预改变老年人肠道菌群从而降低衰弱状态和改善健康状况
期刊名:Gut
影响因子:17.9
发表时间:2020年
发表单位:爱尔兰科克大学APC微生物研究所
目标: 衰老伴随着多种身体功能的退化和炎症,这些共同导致衰弱。已有研究证明,衰弱与肠道微生物群的改变是共变的,这种变化是通过饮食多样性受限性而加速的。地中海饮食与健康有关。在地中海饮食NU-AGE试验中,调查了地中海饮食干预一年时间是否可以改变受试者的肠道菌群,从而降低衰弱状态。
设计:对欧洲五个国家(英国、法国、荷兰、意大利和波兰)共计612名老年非衰弱受试者和老年衰弱前期受试者进行了为期一年的地中海饮食干预,然后对饮食干预前后的肠道菌群进行了分析。
结果:坚持地中海饮食与特定微生物群的改变有关。坚持地中海饮食而富集的微生物与一些降低衰弱和认知功能改善的标志物呈正相关,与炎症标志物包括c-反应蛋白和白细胞介素-17呈负相关。对微生物代谢产物谱的分析表明,地中海饮食调节的肠道菌群变化与短链/支链脂肪酸产量增加和次级胆汁酸、对甲酚、乙醇和二氧化碳产量降低有关。微生物群落生态系统共现性网络分析表明,对地中海饮食干预有积极反应的细菌类群占据互作网络的关键位置,而衰弱相关菌群则处于互作网络的外围。
结论:总体而言,该研究结果支持通过改善饮食习惯以调节肠道菌群的可行性,而肠道菌群又有可能促进更健康的衰老变化。
研究背景:
伴随衰老而来的衰弱包括多种生理系统的衰竭和先天性的持续激活免疫炎症反应。衰弱可能包括与老化相关的炎症、认知功能丧失、肌肉减少以及糖尿病和动脉粥样硬化等慢性疾病的发生发展。改变饮食模式,如采用地中海饮食(MedDiet)已被认为是解决衰弱的主要治疗策略。地中海饮食的特点是蔬菜、豆类、水果、坚果、橄榄油和鱼的食用增加,红肉、乳制品和饱和脂肪的食用减少。坚持地中海饮食与降低死亡率、增加抗氧化活性、降低数种疾病的发病率以及减少炎症有关。数项研究表明,坚持地中海饮食的依从性与降低衰弱有关。除了降低疾病发生外,坚持地中海饮食还与肠道微生物组分的有益变化相关,例如导致变形杆菌丰度降低,短链脂肪酸的产生水平增加。在全球范围内,大多数老年人不采用地中海饮食,事实上,老年保健的一个主要挑战是采用与肠道微生物多样性降低相关的限制性饮食,特别是在长期居住护理的受试者中。地中海饮食NU-AGE干预项目旨在研究在一个来自五个不同的国家(波兰、荷兰、英国、法国和意大利)超过1200名年龄在65-79岁之间的老年人的大队列中,使用定制膳食12个月的效果。这项研究的基线和干预后结果报告了检测到的代谢物和身体成分数据在性别和国籍上的差异,研究发现,坚持地中海饮食的依从性与整体认知和情景记忆能力提高之间存在显著关联;此外,更高的地中海饮食依从性可以降低骨质疏松症患者的骨丢失及改善先天免疫功能。
NU-AGE试验的参与者包括612名个体,包括289名对照者(145名男性和144名女性)和323名NU-AGE饮食受试者(141名男性和182名女性),在本研究中,分析了地中海饮食对这些参与者肠道微生物群落的影响,结果发现各种有益的结果与肠道微生物群落的改变相关。
研究结果:
饮食和微生物组群在基线水平上具有共变性和差异性
基于饮食的主坐标分析(PCoA)表明,在基线水平上,三个不同国家之间存在显著的饮食差异(图1A):第一个亚组包含意大利受试者;第二个亚组包含英国和法国受试者;第三个亚组包含荷兰和波兰受试者。
总体而言,在基线和1年后共收集了612人(对照组和干预组)配对微生物组数据。基于用16S rDNA OTUs的PCoA分析(基于Spearman距离)在基线水平上也观察到类似的聚类模式(图1B):意大利受试者的微生物组分明显不同,但来自英国/法国和波兰/荷兰的受试者更相似。基于食物消耗和OTU丰度分布的Procrustes分析证实了饮食与微生物组分之间存在显著相关性,特定微生物在基线水平上促进了不同国家的差异(Mann-Whitney检测)。
正如预期的那样,饮食干预组与对照组有显著差异(图1C)。饮食干预组的这些变化主要是由纤维、维生素(C、B6、B9、硫胺素)和矿物质(铜、钾、铁、锰、镁)摄入量的增加引起的,而对照组的变化则与脂肪摄入量(饱和脂肪和单不饱和脂肪酸)的增加有关(图1D)。
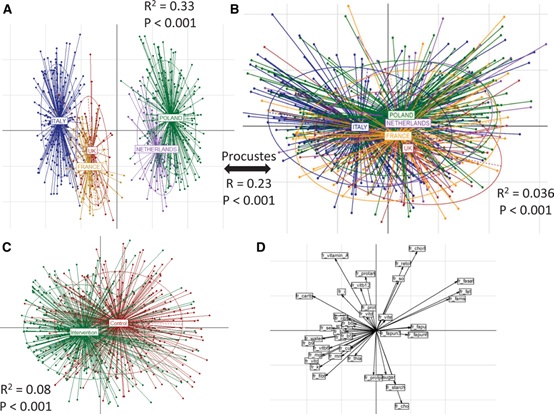
图1基线期习惯性饮食和微生物群组成因国家而异,饮食干预改变了宏观营养状况
增加对地中海饮食的依从性会影响与健康相关的肠道特定菌群
在整个研究中,观察到地中海饮食依从性增加与减少微生物多样性的损失有关(表1)。为了进行更详细的微生物群-饮食关联分析,基于FBDG饮食指南计算了地中海饮食依从性得分;同时建立了随机森林(RF)模型,基于微生物群预测地中海饮食依从性得分。对于这两种模型,基于微生物群预测得到的地中海饮食依从性得分与基于实际食物的得分之间的相关性显著,表明肠道菌群与坚持地中海饮食之间存在明显的关联。在确定对地中海饮食有响应的肠道菌群过程中,75个OTUs的组合具有最好的预测性能,称之为“饮食响应”OTUs/分类群/标记物。总的来说,使用这组OTUs预测的饮食依从性得分和实际观察到的饮食依从性得分之间的相关性为0.39(图2A)。
共有44个预测OTUs与地中海依从性得分呈正相关,45个预测OTUs与地中海依从性得分呈负相关,分别称之为“饮食阳性”和“饮食阴性”OTUs(图2B)。这两个组的微生物类群是不同的,“饮食阳性”OTUs主要归类为Faecalibacterium prausnitzii、以及Roseburia (R. hominis) 、Eubacterium (E.rectale, E. eligens, E. xylanophilum) 等。这些分类群中的大多数以前都报到过与健康相关,包括短链脂肪酸(SCFAs)的产生和抗炎特性,以及与2型糖尿病和结直肠癌等疾病负相关。与之相反,“饮食阴性”OTUs主要为Ruminococcus torques, Collinsella aerofaciens等,而这些菌的大量增加与2型糖尿病和结直肠癌、动脉粥样硬化、肝硬化和炎症性肠病有关。这些发现表明坚持地中海饮食有可能在与健康正相关的方向上调节肠道菌群。值得注意的是,尽管在基线水平(图1B)和不同的饮食依从性上存在因为国家不同而造成的微生物组组成差异,但在整个队列中确定的对地中海饮食响应的微生物群在不同民族之间共享的,也就是说,这些对地中海饮食响应的微生物群与饮食的关联是不受国籍影响的。通过比较饮食干预组和对照组以及通过增加对饮食的依从性确定的这些微生物丰度的变化模式(图2C,D),进一步验证了这些微生物群与地中海饮食依从性的关系。
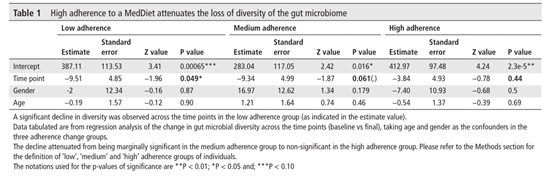
表1 增加对地中海饮食的依从性与降低微生物多样性的损失有关
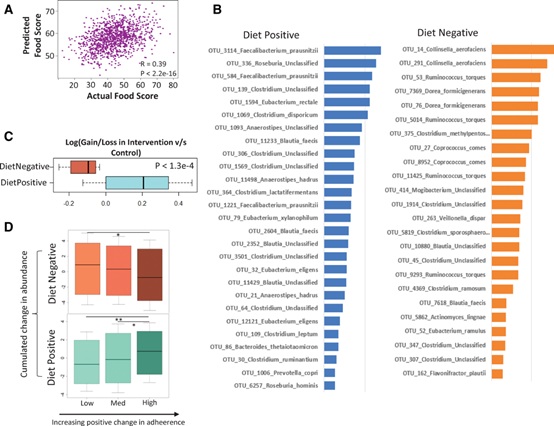
图2 通过机器学习识别地中海饮食响应微生物类群
地中海饮食干预调节与衰弱和炎症负相关的肠道菌群
地中海饮食干预的主要目标是减少衰弱和出现炎症,因此研究对象根据评分分为非衰弱(或明显健康)、前脆弱和脆弱组。“饮食阴性”微生物随三个衰弱组(即衰弱组>前衰弱组>非衰弱组)呈逐步显著下降趋势,而“饮食阳性”微生物在健康组(非衰弱组)中的丰度显著升高,“饮食阳性”微生物在衰弱程度减轻的个体中显示出显著的增加。然而不能观察到地中海饮食依从性和衰弱之间的直接联系,因此推断饮食依从性对衰弱的影响可能是间接的,因此,增加对地中海饮食的依从性可能会调节肠道菌群,并且这些菌群的反应可能与与衰弱的减弱或降低衰弱的风险直接相关。
为了调查这一点,计算了整个研究队列中对地中海饮食响应的OTUs标记物与衰弱、认知功能和炎症的相关指数之间的关联,总的来说,我们观察到饮食阳性和饮食阴性OTUs与五种不同的细胞因子/生物标记物(即促炎性高敏C反应蛋白hsCRP,白细胞介素17(IL-17),抗炎性sGP130以及脂联素和瘦素),三项与衰弱相关的测量指标(Fried评分、握力和步速时间),以及与认知功能相关BabCock记忆评分和结构练习的关联模式存在显著差异:饮食阳性的OTU标记与炎症标记hsCRP和IL-17水平以及Fried评分和步态速度时间(两项指标均与衰弱程度增加相关)呈一致的负相关;相反,它们与认知功能改善指标(如结构练习、BabCock记忆评分)、衰弱程度降低指标(握力)和两种细胞因子(脂联素和sGP130)的测量结果呈一致的正相关(图3A)。值得注意的是,尽管在饮食摄入、微生物组分和依从性得分方面存在国家差异,这些关联中的每一个(BabCock记忆评分除外)至少可以在三个以上国家重现性比较好(图3B)。这些结果清楚地表明,坚持地中海饮食与微生物群调节的相关性在各个国家较为一致,反过来坚持地中海饮食又与降低衰弱程度、改善认知功能和减轻炎症相关。
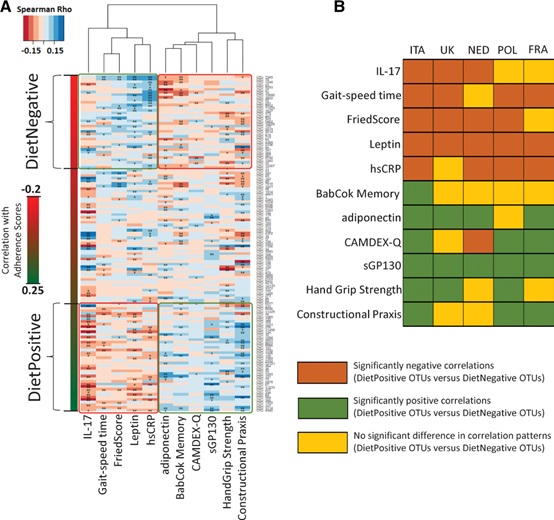
图3饮食响应微生物类群与衰弱、认知功能和炎症指标的关联分析
肠道菌群响应,伴随代谢谱的有益变化,是饮食依从性和健康之间的关键中间环节
根据前面的发现,似乎与饮食依从性相关的微生物群落对于改善健康状况比仅仅依从饮食本身更为重要。地中海饮食的特点是特定饮食成分的消费模式发生变化,即纤维(蔬菜、水果)、碳水化合物(全麦)、植物蛋白(豆类)、多不饱和脂肪酸(鱼类)和维生素C(水果)的消费量增加,同时减少食用肉类、酒、盐和糖。我们首先通过检测了地中海饮食响应OTUs与具有不同食物成分饮食模式的相关性,结果观察到,饮食响应OTU标记与FBDG预测的饮食依从性得分正相关,表明其与纤维、维生素C、维生素D、植物蛋白和碳水化合物正相关,与酒精、脂肪和糖组分负相关,因此上述结果表明,OTU标记不仅与FBDG预测的饮食依从性得分相关,而且与地中海饮食干预的个体膳食成分相关。
基于饮食相关OTUs标记与地中海饮食依从性得分的总体相关性,我们计算了地中海饮食调节的微生物组分指数。正如预期的那样,地中海饮食微生物组分指数与总体饮食依从性得分呈正相关,也反映了单个OTUs标记的总体关联模式(即与纤维、碳水化合物、植物蛋白、维生素C、多不饱和脂肪酸呈正相关,与脂肪、酒精和糖呈负相关),表明其作为与地中海饮食相关标记的有效性。
然后将地中海饮食依从性得分作为混杂因素,检查该地中海饮食微生物组分指数与衰弱、认知功能和炎症的不同测量指标的相关性。11种与改善认知、减轻衰弱和炎症有关的指标中,有10种可以重现,还观察到地中海饮食微生物组分指数与炎症相关的细胞因子白细胞介素(IL)-2和巨噬细胞炎症蛋白(MIP)-1b呈负相关,与语言流畅性呈正相关(图4)。这些结果表明,地中海饮食调节的微生物组分与衰弱、炎症和认知功能相关,并且这种相关与依从性得分无关(即这些不是与饮食依从性相关的间接后果)。接下来,检查了混杂因素(如年龄、体重指数、性别、疾病病理生理学和药物摄入)对饮食-微生物分类单元关联程度的影响,与非患病对照组相比,患有多种疾病的个体,特别是糖尿病、心脏病发作和炎症性疾病的个体,其微生物组分显著降低,然而即使考虑到包括年龄、体重指数、性别和不同疾病病理生理学的所有混杂因素,微生物组分指数与10种炎症标志物和7种衰弱指数的关联模式基本保持不变(如图4所示)。
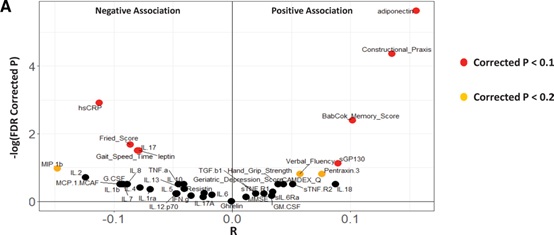
图4 地中海饮食调节的微生物组分指数与衰弱程度降低、认知功能改善和炎症减轻相关,但是与饮食依从性评分无关
饮食调节的微生物群变化对健康状况的积极影响可能是由特定的微生物代谢产物驱动的。考虑到粪便代谢数据对个体不可用,我们使用相应的16S物种组成谱预测肠道微生物组的代谢谱。然后将这些预测代谢谱丰度的跨时间点变化与微生物组指数变化进行关联分析,结果发现“饮食阳性”微生物的变化与微生物消耗纤维相关的非淀粉多糖的增加有关(可能表明地中海饮食的变化),相反,“饮食阴性”微生物的变化与微生物单糖消耗增加有关。微生物群呈阴性反应时,胆汁酸的牛磺酸和糖类衍生物通过胆酸和鹅去氧胆酸消耗到次级胆汁酸(石胆酸、脱氧胆酸)的量也会增加,而总所周知胆汁酸调节失调与不同的疾病条件有关,特别是石胆酸和脱氧胆酸的产生增加与结直肠癌有关。相反,支链脂肪酸(BCFAs)和SCFAs产量的增加与微生物群的阳性反应有关,SCFAs与宿主健康之间的正相关是公认的。此外,在目前的研究中,我们获得了意大利和波兰队列中的一部分个体的血浆胆酸(CA)、乙醇鹅去氧胆酸(GDCDA)和鹅去氧胆酸(CDCA)水平的测量数据。对于GCDCA和CDCA,这些胆汁酸的血浆水平与饮食相关标记物的丰度相关显示出如下趋势:与饮食阴性OTUs相比,饮食阳性OTUs与GCDCA水平的正相关性显著增强,与CDCA水平的负相关性增强。根据GDCDA/CDCA比率,将这部分个体分成三组,观察到GCDCA/CDCA比值增加的个体,其饮食相关微生物群指数显著正相关。这些结果证实在这些代谢物谱中,随着饮食相关微生物群指数的增加,预测个体的GDCDA到CDCA的微生物转化率降低,从而导致GDCDA/CDCA水平升高。阴性微生物群反应也与其它有害代谢物,如对甲酚、乙醇和二氧化碳,而其相对产生过剩与结直肠癌、胰岛素抵抗、非酒精性脂肪肝、细胞毒性和小肠细菌过度生长有关。值得注意的是,在基线水平上,地中海饮食相关微生物群指数与多种疾病(包括高血压、糖尿病和癌症)呈负相关。因此这些结果表明,与阳性微生物群反应相关的代谢变化有益于宿主健康。
饮食阳性OTUs是肠道群落中的关键物种
最后,我们评估了饮食反应类群在整个微生物群落结构中的作用。在共现网络中,节点表示分类群OTUs,节点之间的边表示它们之间的显著共现关系。类群OTUs在共生网络中的位置表明了类群OTUs在群落稳定性中的相对重要性。我们首先得到了两个队列的所有跨时间点样本的共现网络。然而,大多数饮食阳性OTUs和饮食阴性OTUs的位置有着显著的不同。饮食阳性OTUs要么位于网络中心,要么作为主要子节点内的连接节点(图5A),这表明了这些分类群在肠道群落结构中的中心地位,这种分类群被称为“关键物种”。与此相反,大多数饮食阴性OTUs位于网络的边缘。
我们通过计算网络中每个分类单元的两个中心度度量来探讨这一现象:“中心度”(degree centrality)是连接到特定节点的节点数,而“中间中心度”(betweenness centrality)是通过特定节点连接任意两个节点的路径数。与饮食阴性OTUs或非相关标记相比,饮食阳性OTUs具有更高的中间中心度(betweenness centrality)(图5B,C)。我们在每一个不同的国家内以及在不断增加饮食依从性样本的重叠窗口中重新建立了这个网络。尽管个体网络的总体结构存在重大差异,但无论在哪个国家,分类群的分布模式及其在肠道微生物网络中的相对重要性都是不变的。无论民族和个体的饮食依从性如何,饮食阳性OTUs都具有显著较高的中心度(degree centrality)。正如预期的那样,饮食阳性OTUs和饮食阳性OTUs也有不同的相互作用模式,特别是iBBiG分析鉴别到的衰弱相关模块C,它与饮食阳性OTUs有负的共现趋势(图5D)。有趣的是,随着饮食依从性的增加,共现倾向的强度变得明显更为消极(图5E),而其它任何分类模块都没有发现这种情况。
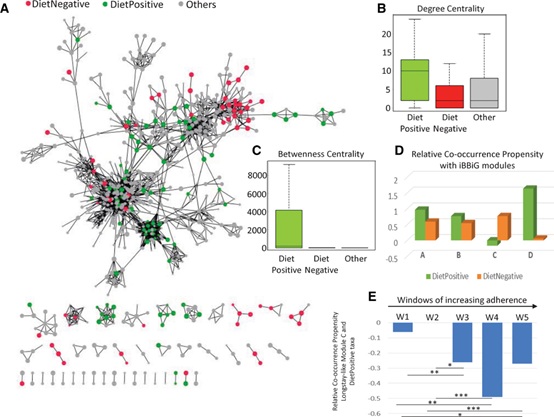
图5对地中海饮食干预有阳性反应的细菌类群占据了微生物群网络中与衰弱相关类群的关键互作节点。